El nuevo virus humano emergente SARS-CoV-2 está resultando en altas tasas de mortalidad y sistemas de salud incapacitados. Prevenir una mayor transmisión es una prioridad.
Abstracto
El nuevo virus humano emergente SARS-CoV-2 está resultando en altas tasas de mortalidad y sistemas de salud incapacitados. Prevenir una mayor transmisión es una prioridad. Analizamos los parámetros clave de la propagación de la epidemia para estimar la contribución de las diferentes rutas de transmisión y determinar los requisitos de aislamiento de casos y rastreo de contactos necesarios para detener la epidemia. Concluimos que la propagación viral es demasiado rápida para ser contenida por el rastreo manual de contactos, pero podría controlarse si este proceso fuera más rápido, más eficiente y sucediera a escala. Una aplicación de rastreo de contactos que crea una memoria de contactos de proximidad y notifica inmediatamente a los contactos de casos positivos, puede lograr el control de la epidemia si es utilizada por suficientes personas. Al dirigir las recomendaciones solo a las personas en riesgo, Las epidemias podrían ser contenidas sin necesidad de cuarentenas masivas (“bloqueos”) que son perjudiciales para la sociedad. Discutimos los requisitos éticos para una intervención de este tipo.
Artículo originalmente publicado en la revista Science – www.sciencemag.org
COVID-19 es una enfermedad infecciosa de rápida propagación causada por el nuevo coronavirus SARS-COV-2, un betacoronavirus, que ahora ha establecido una pandemia global. Alrededor de la mitad de las personas infectadas se convierten en casos reportados, y con el apoyo de cuidados intensivos, la tasa de letalidad es aproximadamente del 2% ( 1 ).
Más preocupante es que la proporción de casos que requieren apoyo de cuidados intensivos es del 5%, y el manejo del paciente se complica por los requisitos para usar equipo de protección personal y participar en procedimientos de descontaminación complejos ( 2 ).
Es probable que las tasas de mortalidad sean más altas en las poblaciones de más edad que en la provincia de Hubei (como en Europa), y en entornos de bajos ingresos donde faltan instalaciones de cuidados críticos ( 3 ).
En (4) el costo para la salud pública de no lograr una supresión epidémica sostenida se estimó en 250,000 vidas perdidas en los próximos meses en Gran Bretaña, y 1.1-1.2 millones en los Estados Unidos, incluso con la acción de mitigación más fuerte posible para ‘aplanar la curva’.
Incluso los brotes modestos verán aumentar las tasas de mortalidad a medida que se sobrepase la capacidad del hospital, y los efectos indirectos causados por servicios de atención médica comprometidos aún no se han cuantificado.
Actualmente no hay tratamiento disponible, y una vacuna no estará disponible durante varios meses (a partir de marzo de 2020) como mínimo. Los únicos enfoques que actualmente tenemos disponibles para detener la epidemia son los del control clásico de la epidemia, como el aislamiento de casos, el rastreo de contactos y la cuarentena, el distanciamiento físico y las medidas de higiene.
El número básico de reproducción R 0 es el número típico de infecciones causadas por un individuo en ausencia de inmunidad generalizada. Una vez que la inmunidad se generaliza, el número efectivo de reproducción R será inferior a R 0 y una vez que R sea inferior a 1, la población tiene inmunidad colectiva y la epidemia disminuye. La inmunidad solo se puede obtener de forma segura mediante la vacunación. Aquí usamos el término “supresión epidémica sostenida” para significar una reducción del número de reproducción R a menos de 1 al cambiar las condiciones no inmunológicas de la población que afectan la transmisión, como los patrones de contacto social.
Los detalles biológicos de la transmisión de los betacoronavirus se conocen en términos generales: estos virus pueden pasar de un individuo a otro a través de gotitas exhaladas ( 5 ), aerosol ( 6 ), contaminación de las superficies ( 7 ) y posiblemente a través de la contaminación fecal-oral ( 8 ) Aquí comparamos diferentes rutas de transmisión que están más estrechamente alineadas con sus implicaciones para la prevención.
Específicamente, proponemos cuatro categorías:
I. Transmisión sintomática: transmisión directa de un individuo sintomático, a través de un contacto que el receptor puede recordar fácilmente.
II. Transmisión pre-sintomática: transmisión: directa de un individuo que ocurre antes de que el individuo fuente experimente síntomas notables. (Tenga en cuenta que esta definición puede ser específica del contexto, por ejemplo, en función de si es la fuente o el destinatario a quien se le pregunta si los síntomas fueron notables).
III. Transmisión asintomática: transmisión directa de individuos que nunca experimentan síntomas notables. Esto solo puede establecerse mediante el seguimiento, ya que la observación de un solo punto de tiempo no puede distinguir completamente a los individuos asintomáticos de los pre-sintomáticos.
IV. Transmisión ambiental: transmisión por contaminación, y específicamente de una manera que normalmente no sería atribuible al contacto con la fuente en una encuesta de contacto (es decir, esto no incluye los pares de transmisión que estuvieron en contacto cercano extendido, pero para quienes en realidad son infecciosos dosis pasada por el medio ambiente en lugar de más directamente). Estos podrían identificarse en un análisis de movimientos espaciales.
Reconocemos que los límites entre estas categorías pueden ser borrosos, pero definidos en términos generales, estas categorías tienen diferentes implicaciones para la prevención, respondiendo de manera diferente a las medidas clásicas de aislamiento de casos y contactos de cuarentena (9, 10) (y para una aplicación específica a COVID-19 ver abajo) (11).
Existe evidencia para cada una de estas rutas de transmisión: sintomática (12), pre-sintomática (13); asintomático (14); y ambiental (12). Para la prevención, la información crucial es la frecuencia relativa de las diferentes rutas de transmisión para asignar recursos finitos entre las diferentes estrategias de intervención.
Li y col . (12) presentaron datos autoinformados sobre la exposición de los primeros 425 casos en Wuhan; Algunas de estas visitas registradas al mercado mayorista de mariscos de Huanan. La generalización de la transmisión en ese entorno a otros entornos es muy incierta, ya que este evento a gran escala sembró la epidemia en ausencia de cualquier conocimiento sobre la enfermedad. Después del cierre del mercado mayorista de mariscos de Huanan el 1 de enero de 2020, de 240 casos sin exposición a ningún mercado húmedo, 200 individuos (83%) informaron que no habían estado expuestos a un individuo con síntomas respiratorios. El recuerdo inexacto puede explicar algunas respuestas, incluyendo no notar que los síntomas eran excepcionales en un momento anterior al comienzo de la conciencia de la enfermedad, pero es poco probable que sea tanto como el 83% de ellos, lo que implica que muchas personas fueron infectadas por personas no sintomáticas.
La situación en Singapur a primera vista parece diferente, ya que a diferencia de Wuhan, muchas personas estaban vinculadas a una fuente sintomática identificada. Sin embargo, la principal diferencia es que el enlace fue retrospectivo, de modo que el enlace podría establecerse incluso si la transmisión se produjo antes de que un caso fuera sintomático. Al 5 de marzo de 2020, había 117 casos, de los cuales 25 fueron importados. Al dedicar recursos considerables, incluida la investigación policial, 75 de los 92 casos de transmisión local se remontan a su supuesta exposición, ya sea a un caso conocido o a un lugar vinculado a la propagación (15) La vinculación de casos a través de una ubicación generalmente incluye la posibilidad de transmisión ambientalmente mediada. Por lo tanto, la gran fracción de transmisión rastreable en Singapur no contradice la gran fracción sin exposición sintomática en Wuhan. Sin embargo, sugiere que la transmisión desde individuos asintomáticos, en lugar de pre-sintomáticos, no es un factor importante de propagación.
Aunque actualmente faltan encuestas serológicas, otras líneas de evidencia sugieren que el escenario de muchas infecciones asintomáticas para cada sintomático es poco probable.
Las pruebas de 1.286 contactos cercanos de casos confirmados encontraron que, entre 98 personas que dieron positivo, solo el 20% no tenía síntomas en la primera evaluación clínica (16). Entre 634 individuos que dieron positivo a bordo del crucero Diamond Princess, se encontró que la proporción de individuos sin síntomas era del 52%; La proporción de asintomáticos (en lugar de pre-sintomáticos) se estimó en 18% (17).
Las pruebas a los pasajeros a bordo de seis vuelos de repatriación desde Wuhan sugieren que entre el 40 y el 50% de las infecciones no se identificaron como casos (4, 18). Se ha encontrado que los casos leves tienen cargas virales 60 veces menos que los casos graves (19) y es probable que las cargas virales de las personas asintomáticas sean aún más bajas, con posibles implicaciones para la infecciosidad y el diagnóstico.
La cuantificación más precisa y robusta de la frecuencia relativa de las rutas de transmisión sería un estudio de cohorte prospectivo bien diseñado con investigaciones detalladas en revistas y filogenéticas. Sin embargo, la emergencia global actual requiere estimaciones oportunas utilizando fuentes de datos imperfectas.
Realizamos un análisis detallado del momento de los eventos en pares de transmisión definidos, obtuvimos la distribución del tiempo de generación y atribuimos una probabilidad para cada par de que la transmisión fuera pre-sintomática.
También ajustamos un modelo matemático de infecciosidad a través de las cuatro rutas discutidas anteriormente, durante el curso de la infección.
Esto nos permitió calcular R 0, estimar la proporción de transmisión desde diferentes rutas y hacer predicciones sobre si el rastreo de contactos y el aislamiento de casos conocidos es suficiente para prevenir la propagación de la epidemia.
Estimación de los parámetros de transmisión del SARS-CoV-2
Utilizamos la tasa de crecimiento exponencial de la epidemia, r , desde las primeras etapas de la epidemia en China, de modo que el efecto de las medidas de control discutidas más adelante será relativo a las primeras etapas de un brote, ejemplificado por los patrones de contacto de referencia y las condiciones ambientales. en Hubei durante ese período.
Notamos que esta suposición está implícita en muchas estimaciones de R 0 . El tiempo de duplicación de la epidemia T 2 es igual a log e (2) / r. Utilizamos el valor r = 0.14 por día (20), correspondiente a un tiempo de duplicación de 5.0 días.
El período de incubación se define como el tiempo entre la infección y el inicio de los síntomas. Se estima como el tiempo entre la exposición y el informe de síntomas notables.
Utilizamos la distribución del período de incubación calculada por (21). La distribución es lognormal con una media de 5,5 días, una mediana de 5,2 días y una desviación estándar de 2,1 días, y se incluye con nuestros resultados en la figura 1.

Panel izquierdo: nuestras distribuciones de tiempo de generación inferidas, en negro; Las líneas más gruesas denotan un mayor soporte para la forma funcional correspondiente, siendo la distribución Weibull la mejor opción. Para la comparación, también incluimos las distribuciones de intervalos en serie reportadas previamente por (12 ) (en azul claro) y (22 ) (en gris), y la distribución del período de incubación que usamos aquí desde (21) (línea roja discontinua). Panel derecho: la distribución de la probabilidad posterior de transmisión pre-sintomática para cada uno de los 40 pares de transmisión. La línea vertical roja muestra la probabilidad media.
El tiempo de generación se define para los pares de transmisión fuente-receptor como el tiempo entre la infección de la fuente y la infección del receptor.
Debido a que generalmente no se conoce el tiempo de infección, el tiempo de generación a menudo se aproxima por el intervalo en serie, que se define como el tiempo entre el inicio de los síntomas de la fuente y el inicio de los síntomas del receptor.
No tomamos ese enfoque aquí; en cambio, estimamos directamente la distribución del tiempo de generación a partir de 40 pares fuente-receptor. Estos pares se seleccionaron manualmente de acuerdo con la alta confianza de transmisión directa inferida de fuentes disponibles públicamente en el momento de la escritura (marzo de 2020), y con un tiempo conocido de aparición de síntomas tanto para la fuente como para el receptor.
Combinamos las fechas de inicio de los síntomas con intervalos de exposición tanto para la fuente como para el receptor (cuando estén disponibles) y la distribución anterior de los tiempos de incubación y de estos se infirió la distribución de los tiempos de generación. La distribución se describe mejor mediante una distribución de Weibull (AIC = 148.4, frente a 149.9 para gamma y 152.3 para distribución lognormal) con media y mediana igual a 5.0 días y desviación estándar de 1.9 días, que se muestra en el panel izquierdo de Fig.1 .
También mostramos los resultados del análisis de sensibilidad a diferentes formas funcionales, y lo comparamos con dos distribuciones de intervalos en serie publicadas previamente en (12 , 22 ). La incertidumbre en el ajuste de la distribución se muestra en la fig. S1 Nuestra distribución es robusta con respecto a la elección de los eventos de transmisión (fig. S2). La correlación en la incertidumbre entre la media inferida y la desviación estándar se muestra en la fig. S3 La distribución de los intervalos en serie para estos pares se muestra en la fig. S4. Los países de los que se obtuvieron los datos del par de transmisión se muestran en la fig. S5
Para cada uno de los 40 pares de transmisión, estimamos la probabilidad posterior de que la transmisión fuera pre-sintomática, es decir, ocurriera antes del inicio de los síntomas en el infector.
Utilizamos un enfoque bayesiano con un previo poco informativo (transmisión antes o después de síntomas igualmente probables).
Las 40 probabilidades inferidas se muestran en el panel derecho de la Fig. 1 ; la probabilidad media es del 37% (IC 95%: 27.5% – 45%), que puede interpretarse como la fracción de los eventos de transmisión pre-sintomáticos de los eventos de transmisión pre-sintomáticos más sintomáticos.
Esta probabilidad media sobre todos los pares se aproxima a nuestra distribución anterior, pero bimodal de probabilidades individuales en la Fig. 1 muestra que estos están típicamente lejos de lo anterior, es decir, los datos son muy informativos. La incertidumbre en el valor de esta fracción se muestra en la fig. S6. El valor no depende significativamente de la elección de la forma funcional anterior (figs. S7 y S8) de la distribución de tiempos de generación (figs. S9 y S10), ni de la elección de los eventos de transmisión (fig. S11).
Un modelo matemático general de infecciosidad por SARS-CoV-2
Utilizamos un formalismo matemático ( 23 ) que describe cómo la infecciosidad varía en función del tiempo desde la infección, τ, para una cohorte representativa de individuos infectados. Esto incluye la heterogeneidad entre individuos y promedios sobre aquellos individuos que infectan a otros pocos y aquellos que infectan a muchos. Este promedio define la función β (τ).
La infecciosidad puede cambiar con τ debido tanto a los cambios en la biología de la enfermedad (especialmente a la eliminación viral) como al cambio en el contacto con otros. El área bajo la curva β es el número de reproducción R 0 .
Descomponemos β (τ) en cuatro contribuciones que reflejan nuestra categorización anterior, a saber, transmisión asintomática, transmisión pre-sintomática, transmisión sintomática y transmisión ambiental.
El área bajo la curva de una de estas contribuciones da el número total medio de transmisiones sobre una infección completa, a través de esa ruta – asintomática, pre-sintomática, sintomática o ambiental – que definimos como R A , R P , R S y R E respectivamente. La suma de estos es R 0 .
La fórmula matemática para β (τ) es:
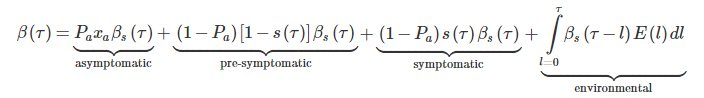
β s (τ) es la infecciosidad de un individuo actualmente sintomático o pre-sintomático, a la edad de infección τ. Otros parámetros en esta expresión, y aquellos que la alimentan indirectamente, se enumeran en la Tabla 1 .
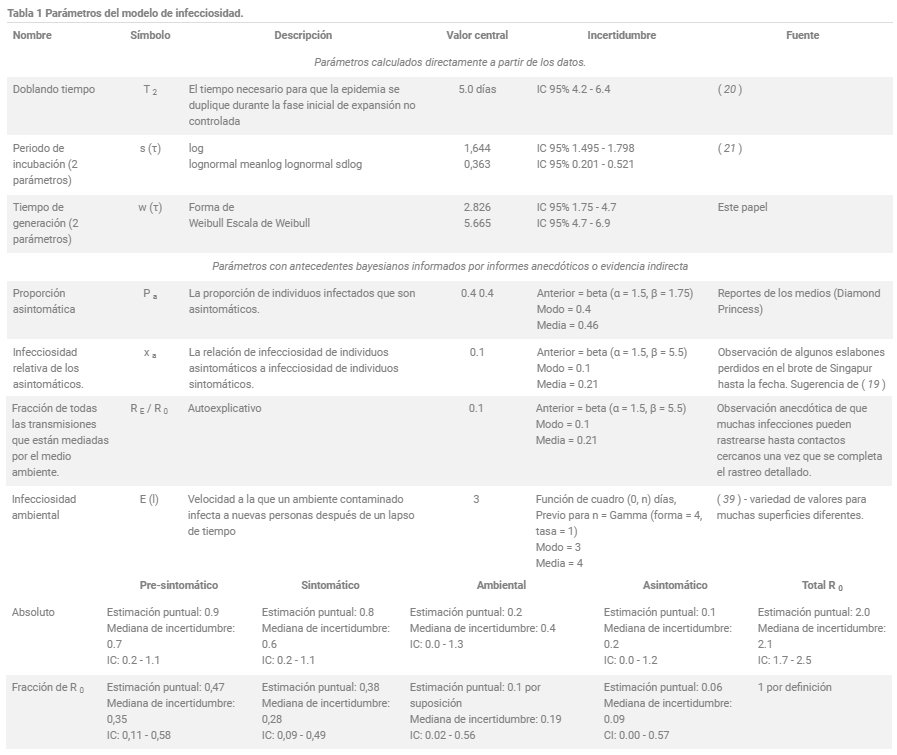
Una discusión detallada de esta expresión, incluidos sus supuestos, se encuentra en los materiales complementarios. Los antecedentes elegidos para los parámetros no calculados directamente a partir de los datos se muestran en la fig. S12. El resultado del modelo de infecciosidad utilizando valores centrales de todos los parámetros se muestra en la figura 2.
Tabla 1. Parámetros del modelo de infecciosidad.
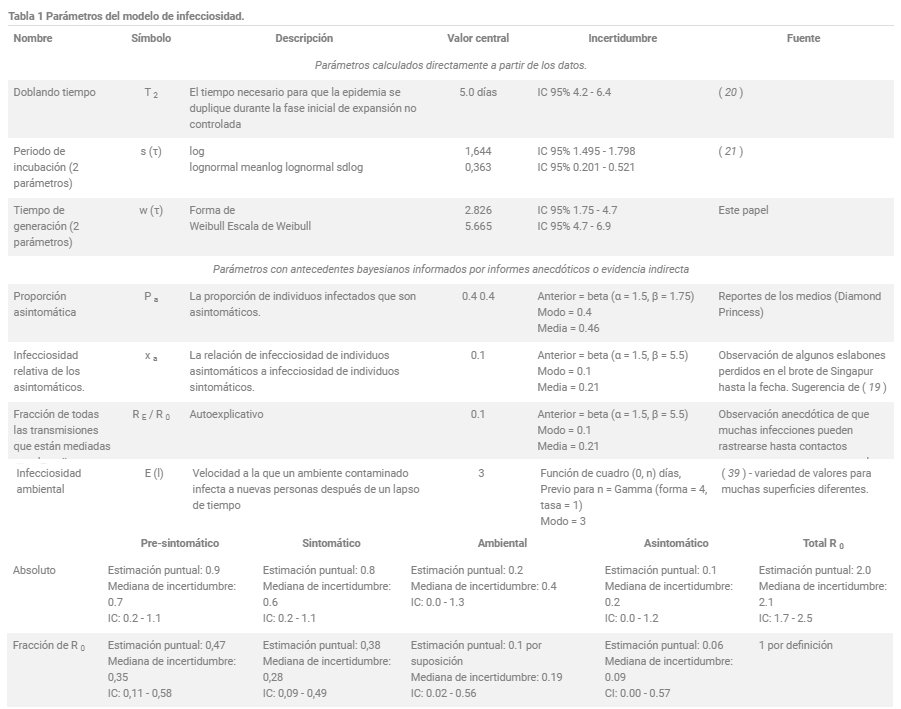
Figura 2. Nuestro modelo de infecciosidad.

Los valores se redondean a un decimal. La detención de la propagación de la enfermedad requiere la reducción de R a menos de 1: bloqueo de la transmisión, de cualquier combinación de colores y valores de τ que podamos lograr, de modo que el área total se reduzca a la mitad.
Al extraer conjuntos de parámetros de entrada de las incertidumbres que se muestran en la Tabla 1, cuantificamos nuestra incertidumbre en R 0 y sus cuatro contribuciones. Los valores resultantes se muestran en la Tabla 2 y sus distribuciones subyacentes se muestran en la fig. S13. Las distribuciones bidimensionales que muestran correlaciones en la incertidumbre se muestran en la fig. S14.
Tabla 2 R 0 y sus componentes.
La estimación de R P / (R P + R S ) obtenida por este método es 0.55 (0.37 – 0.72), que es mayor que la estimación de 0.37 (0.28 – 0.45) de nuestro análisis de los 40 pares de transmisión pero con incertidumbre superpuesta .
Definimos θ como la fracción de todas las transmisiones que no provienen del contacto directo con un individuo sintomático: 1 – R S / R 0 . Esto corresponde al θ de (9) en el caso en que solo hay transmisión pre-sintomática y sintomática. De la Tabla 2 esto es 0.62 (0.50 – 0.92). El valor de θ observado durante una epidemia de crecimiento exponencial se distorsionará cuando el momento de las diferentes contribuciones a la transmisión ocurra en diferentes etapas de la infección, debido a la sobrerrepresentación de individuos recientemente infectados.
Este efecto puede calcularse mediante el uso de la ecuación de renovación, como se hizo recientemente para calcular la distribución del tiempo desde el inicio de los síntomas de COVID-19 hasta la recuperación o la muerte (20) (ver materiales complementarios). Calculamos el θ que se observaría con el crecimiento exponencial temprano visto en China como 0.68 (0.56 – 0.92). La corrección debida a la dinámica de la epidemia es pequeña en comparación con las incertidumbres de los parámetros.
Desarrollamos nuestro modelo matemático de infecciosidad en una aplicación web donde los usuarios pueden probar el efecto de combinaciones alternativas de parámetros (24).
Modelado de aislamiento de casos y seguimiento de contratos con cuarentena
Modelamos el impacto combinado de dos intervenciones: (i) aislamiento de individuos sintomáticos y (ii) rastrear los contactos de casos sintomáticos y ponerlos en cuarentena. Estas intervenciones tienen como objetivo detener la propagación del virus al reducir la cantidad de transmisiones tanto de individuos sintomáticos como de sus contactos (que pueden no ser sintomáticos), al tiempo que minimizan el impacto en la población en general.
En la práctica, ninguna intervención será exitosa o posible para el 100% de los individuos. La tasa de éxito de estas intervenciones determina la evolución a largo plazo de la epidemia.
Si las tasas de éxito son lo suficientemente altas, la combinación de aislamiento y rastreo / cuarentena de contactos podría llevar a R por debajo de 1 y, por lo tanto, controlar eficazmente la epidemia.
Un marco matemático analítico para el impacto combinado de estas dos intervenciones en una epidemia se derivó previamente en (9). En el material complementario, resolvemos estas ecuaciones utilizando nuestro modelo de infecciosidad anterior, es decir, cuantificando cómo se espera que se controle o no la epidemia de SARS-CoV-2 mediante el aislamiento de casos y la cuarentena de contactos trazados. Nuestros resultados se muestran en la Fig. 3. La línea negra muestra el umbral para el control de la epidemia: las tasas de éxito combinadas en la región en la parte superior derecha de la línea negra son suficientes para reducir R a menos de uno.
La xaxis es la tasa de éxito del aislamiento de casos, que puede considerarse como la fracción de individuos sintomáticos aislados, suponiendo una prevención perfecta de la transmisión en el aislamiento, o el grado en que la infecciosidad de los individuos sintomáticos se reduce suponiendo que todos estén aislados. El eje y es la tasa de éxito del rastreo de contactos; Del mismo modo, esto puede considerarse como la fracción de todos los contactos rastreados, suponiendo una cuarentena perfectamente exitosa al rastrear, o el grado en que se reduce la infecciosidad de los contactos, suponiendo que se rastrean todos. Estos resultados para la efectividad de la intervención, y su dependencia de todos los parámetros en nuestro análisis combinado, pueden explorarse a través de la misma interfaz web que para nuestro modelo de infecciosidad (24).
Fig. 3 Cuantificación del éxito de la intervención .
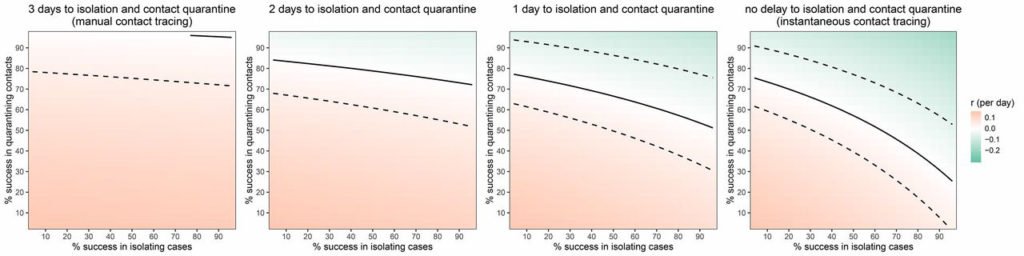
r en función de la tasa de éxito del aislamiento instantáneo de casos sintomáticos (eje x) y la tasa de éxito del rastreo de contacto instantáneo (eje y). Los valores positivos de r (rojo) implican una epidemia creciente; Los valores negativos de r (verde) implican una epidemia decreciente, con valores negativos mayores que implican una disminución más rápida. La línea negra continua muestra r = 0, es decir, el umbral para el control de la epidemia. Las líneas discontinuas muestran incertidumbre en el umbral debido a la incertidumbre en R0 (ver figs. S15 a S17). Los diferentes paneles muestran variaciones en el retraso asociado con la intervención, desde el inicio de los síntomas hasta el aislamiento de casos y la cuarentena de los contactos.
Las demoras en estas intervenciones los hacen ineficaces para controlar la epidemia ( Fig. 3 ): los procedimientos tradicionales de localización manual de contactos no son lo suficientemente rápidos para el SARS-CoV-2. Sin embargo, un retraso desde la confirmación de un caso hasta la búsqueda de sus contactos no es inevitable. Específicamente, este retraso puede evitarse utilizando una aplicación de teléfono móvil.
Control epidémico con seguimiento de contacto digital instantáneo.
Una aplicación de teléfono móvil puede hacer que el seguimiento de contactos y la notificación sean instantáneos tras la confirmación del caso. Al mantener un registro temporal de eventos de proximidad entre individuos, puede alertar inmediatamente a los contactos cercanos recientes de casos diagnosticados y hacer que se autoaislen.
Se han implementado aplicaciones con objetivos similares en China. La política de salud pública se implementó utilizando una aplicación que no era obligatoria pero que se requería para moverse entre los barrios y los espacios públicos y el transporte público.
La aplicación permite que una base de datos central recopile datos sobre el movimiento del usuario y el diagnóstico de coronavirus y muestra un código verde, ámbar o rojo para relajar o imponer restricciones al movimiento. Se informa que la base de datos es analizada por un algoritmo de inteligencia artificial que emite los códigos de color ( 25 ). La aplicación es un complemento para las aplicaciones WeChat y Alipay y, en general, se ha adoptado.
China continental fuera de la provincia de Hubei recibió significativamente más presentaciones de Wuhan que en cualquier otro lugar, después de los movimientos masivos de personas en torno al Año Nuevo chino y el inicio del bloqueo de Wuhan ( 26 ). A pesar de esto, se ha logrado una supresión epidémica sostenida en China: se han reportado menos de 150 casos nuevos cada día del 2 al 23 de marzo, frente a miles cada día en el apogeo de la epidemia.
Corea del Sur también ha logrado una supresión epidémica sostenida: 76 casos nuevos el 24 de marzo, frente a un pico de 909 el 29 de febrero, y también está utilizando una aplicación de teléfono móvil para recomendar la cuarentena.
Tanto las aplicaciones chinas como las surcoreanas han sido objeto de escrutinio público por cuestiones de protección de datos y privacidad.
Dado que nuestro resultado en la Fig. 3 implica la necesidad de un rastreo de contactos extremadamente rápido, nos propusimos diseñar un algoritmo simple y ampliamente aceptable a partir de los primeros principios epidemiológicos, utilizando la funcionalidad común de los teléfonos inteligentes. El método se muestra en la Fig. 4 . La funcionalidad principal es reemplazar el trabajo de una semana de rastreo manual de contactos con señales instantáneas transmitidas desde y hacia un servidor central. Los diagnósticos de coronavirus se comunican al servidor, lo que permite recomendar cuarentena estratificada por riesgo y medidas de distanciamiento físico en aquellos que ahora se sabe que son posibles contactos, al tiempo que se preserva el anonimato del individuo infectado. Las pruebas pueden ser solicitadas por personas sintomáticas a través de la aplicación.
Fig. 4 Un esquema del rastreo de contactos COVID-19 basado en aplicaciones.
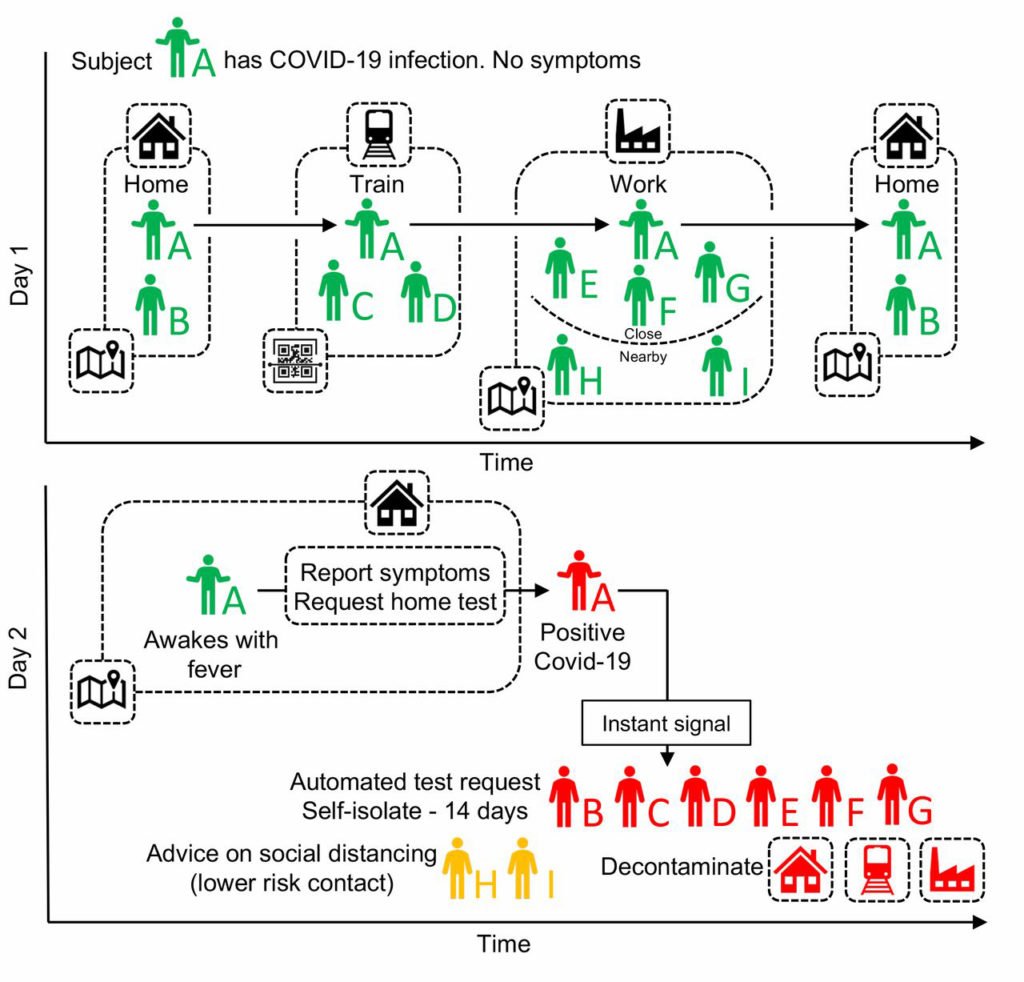
La persona A solicita una prueba de SARS-COV-2 (usando la aplicación) y el resultado positivo de su prueba desencadena una notificación instantánea a las personas que han estado en contacto cercano.
La aplicación aconseja el aislamiento del caso (individuo A) y la cuarentena de sus contactos.
El algoritmo simple se puede refinar fácilmente para que sea más informativo, por ejemplo, poner en cuarentena las áreas si las epidemias locales se descontrolan, poner en cuarentena a hogares enteros o realizar un seguimiento de contactos de segundo o tercer grado si el número de casos aumenta, lo que resultaría en que más personas sean preventivamente en cuarentena.
Las recomendaciones algorítmicas también pueden anularse manualmente, donde los funcionarios de salud pública reúnen evidencia más específica. La aplicación puede servir como el centro central de acceso a todos los servicios de salud, información e instrucciones de COVID-19, y como un mecanismo para solicitar entregas de alimentos o medicamentos durante el autoaislamiento.
En el contexto de una aplicación de teléfono móvil, la Fig. 3 pinta una imagen optimista. No hay demora entre la confirmación del caso y la notificación de los contactos, dejando la demora total para el proceso de cuarentena del contacto como la de un individuo que inicia los síntomas hasta su confirmación como caso, más la demora para que los contactos notificados entren en cuarentena.
El retraso entre el desarrollo de los síntomas y la confirmación del caso disminuirá con protocolos de prueba más rápidos, y de hecho podría volverse instantáneo si el diagnóstico presuntivo de COVID-19 basado en los síntomas fuera aceptado en áreas de alta prevalencia.
La demora entre la notificación de los contactos y la entrada en cuarentena debe ser mínima con altos niveles de comprensión pública, al igual que la demora para el aislamiento del caso.
La eficacia del rastreo de contacto (el eje y de La figura 3 ) se puede identificar con el cuadrado de la proporción de la población que usa la aplicación, multiplicado por la probabilidad de que la aplicación detecte contactos infecciosos, multiplicado por la reducción fraccional de la infecciosidad resultante de ser notificado como contacto.
Consideraciones éticas
El uso exitoso y apropiado de la aplicación se basa en que tiene una confianza pública bien fundada. Esto se aplica al uso de la aplicación en sí y de los datos recopilados.
Existen argumentos éticos sólidos y bien establecidos que reconocen la importancia de lograr beneficios para la salud y evitar daños. Estos argumentos son particularmente fuertes en el contexto de una epidemia con el potencial de pérdida de vidas en la escala posible con COVID-19.
Es probable que los requisitos para que la intervención sea ética y capaz de exigir la confianza del público comprenden lo siguiente:
- Supervisión por una junta asesora inclusiva y transparente, que incluye a miembros del público.
- El acuerdo y la publicación de principios éticos por los cuales se guiará la intervención.
- Garantías de equidad de acceso y tratamiento.
- El uso de un algoritmo transparente y auditable.
- Integrar la evaluación y la investigación en la intervención para informar el manejo efectivo de futuros brotes importantes.
- Supervisión cuidadosa y protecciones efectivas en torno a los usos de los datos.
- El intercambio de conocimientos con otros países, especialmente los países de bajos y medianos ingresos.
- Asegurar que la intervención implique la imposición mínima posible y que las decisiones en política y práctica se guíen por tres valores morales: igual respeto moral, equidad y la importancia de reducir el sufrimiento ( especialmente países de bajos y medianos ingresos.
- Asegurar que la intervención implique la imposición mínima posible y que las decisiones en política y práctica se guíen por tres valores morales: igual respeto moral, equidad y la importancia de reducir el sufrimiento ( especialmente países de bajos y medianos ingresos.
- Asegurar que la intervención implique la imposición mínima posible y que las decisiones en política y práctica se guíen por tres valores morales: igual respeto moral, equidad y la importancia de reducir el sufrimiento (27) ecesario y justificado proteger la salud pública.
Es de destacar que el enfoque algorítmico que proponemos evita la necesidad de una vigilancia coercitiva, ya que el sistema puede tener impactos muy grandes y lograr una supresión epidémica sostenida, incluso con una captación parcial.
Las personas deberían tener derecho democrático a decidir si adoptar esta plataforma. La intención no es imponer la tecnología como un cambio permanente a la sociedad, pero creemos que es bajo estas circunstancias pandémicas que es necesario y justificao para poreoteger la salud pública.
Discusión
En este estudio, estimamos parámetros clave de la epidemia de SARS-CoV-2, utilizando un modelo analíticamente solucionable de la fase exponencial de propagación y del impacto de las intervenciones.
Nuestra estimación de R 0 es inferior a muchas estimaciones publicadas anteriormente, por ejemplo ( 12 , 28 , 29 ). Estos estudios asumieron tiempos de generación similares al SARS; sin embargo, la evidencia emergente de tiempos de generación más cortos para COVID-19 implica un R 0 más pequeño. Esto significa que se debe bloquear una fracción menor de las transmisiones para una supresión epidémica sostenida (R <1).
Sin embargo, no significa que la supresión epidémica sostenida sea más fácil de lograr porque las transmisiones de cada individuo ocurren en un período de tiempo más corto después de su infección, y una mayor fracción de ellas ocurre antes de la señal de advertencia de los síntomas. Específicamente, nuestros enfoques sugieren que entre un tercio y la mitad de las transmisiones ocurren en individuos pre-sintomáticos.
Esto está en línea con las estimaciones de que el 48% de la transmisión es pre-sintomática en Singapur y el 62% en Tianjin, China ( 30 ), y el 44% en pares de transmisión de varios países ( 31 ). Nuestro modelo de infecciosidad sugiere que la contribución total a R 0de pre-sintomáticos es 0.9 (0.2 – 1.1), casi suficiente para sostener una epidemia por sí solo. Para el SARS, la estimación correspondiente fue casi cero ( 9 ), lo que nos indicó de inmediato que se necesitarán diferentes estrategias de contención para COVID-19.
La transmisión que ocurre rápidamente y antes de los síntomas, como hemos encontrado, implica que es altamente improbable que la epidemia sea contenida únicamente por el aislamiento de individuos sintomáticos.
Modelos publicados ( 9 – 11 , 32 ) sugieren que en la práctica el estudio de contactos manual sólo puede mejorar esto en un grado limitado: es demasiado lento, y no puede ser ampliado una vez que la epidemia crece más allá de la fase inicial, debido a la limitación de personal.
El uso de teléfonos móviles para medir redes de contacto de enfermedades infecciosas se ha propuesto anteriormente ( 33 – 35) Teniendo en cuenta nuestra cuantificación de la transmisión del SARS-CoV-2, sugerimos que este enfoque, con una aplicación de teléfono móvil que implementa el rastreo instantáneo de contactos, podría reducir la transmisión lo suficiente como para lograr R <1 y una supresión epidémica sostenida, evitando que el virus se propague aún más.
Hemos desarrollado una interfaz web para explorar la incertidumbre en nuestros supuestos de modelado ( 24 ). Esto también servirá como un recurso continuo a medida que nuevos datos estén disponibles y la evolución de la epidemia.
Incluimos la transmisión mediada por el medio ambiente y la transmisión de individuos asintomáticos en nuestro marco matemático general. Sin embargo, la importancia relativa de estas rutas de transmisión sigue siendo especulativa según los datos actuales.
La limpieza y la descontaminación se están implementando en diferentes niveles en diferentes entornos, y las estimaciones mejoradas de su importancia relativa ayudarían a informar esto como una prioridad.
La infección asintomática se ha informado ampliamente para COVID-19, por ejemplo, ( 14 ), a diferencia del SARS donde esto era muy raro ( 36) Argumentamos que los informes de Singapur implican que incluso si las infecciones asintomáticas son comunes, la transmisión hacia adelante desde este estado es probablemente poco común, ya que la reconstrucción forense de las redes de transmisión ha cerrado la mayoría de los enlaces perdidos.
Hay una advertencia importante para esto: el brote de Singapur hasta la fecha es pequeño y no ha implicado a los niños. Se ha especulado ampliamente que los niños podrían ser portadores asintomáticos frecuentes y posibles fuentes de SARS-CoV-2 ( 37 , 38 ).
Calibramos nuestra estimación de la cantidad total de transmisión en función de la tasa de crecimiento de la epidemia observada en China poco después de que comenzara la epidemia. El crecimiento en los países de Europa occidental hasta el momento parece ser más rápido, lo que implica intervalos más cortos entre las personas que se infectan y transmiten en adelante, o un mayor R 0.
Ilustramos el último efecto en las figs. S18 y S19. Si esta es una imagen precisa de la propagación viral en Europa y no un artefacto de crecimiento temprano, el control de la epidemia con solo el aislamiento de casos y la cuarentena de los contactos rastreados parece inverosímil en este caso, lo que requiere un uso de la aplicación casi universal y un cumplimiento casi perfecto.
La aplicación debería ser una herramienta entre muchas medidas preventivas generales de población, tales como distanciamiento físico, mejor higiene de manos y vías respiratorias, y descontaminación regular.
Sin embargo, una intervención basada en aplicaciones podría ser más poderosa de lo que sugiere nuestro análisis aquí. El marco matemático de la ecuación de renovación que utilizamos, aunque está bien adaptado para dar cuenta de una dinámica de infecciosidad realista, no está bien adaptado para dar cuenta de los beneficios de la recursividad en la red de transmisión. Una vez que se han confirmado como casos, las personas identificadas mediante el rastreo pueden desencadenar un mayor rastreo, al igual que sus contactos, etc.
Este efecto no fue modelado en nuestro análisis aquí. Si la capacidad de prueba es limitada, se puede suponer que los individuos que se identifican por rastreo se confirman al inicio de los síntomas, ya que la probabilidad previa de que sean positivos es mayor que para el caso índice, lo que acelera aún más el algoritmo sin comprometer la especificidad.
Con pruebas lo suficientemente rápidas, incluso los casos índice diagnosticados tarde en la infección podrían rastrearse de manera recursiva, para identificar a los individuos recientemente infectados antes de que desarrollen síntomas y antes de que transmitan. La sensibilidad mejorada de las pruebas en la infección temprana también podría acelerar el algoritmo y lograr un control rápido de la epidemia.
El impacto económico y social causado por los bloqueos generalizados es grave. Las personas con bajos ingresos pueden tener una capacidad limitada para permanecer en casa, y el apoyo a las personas en cuarentena requiere recursos.
Las empresas perderán confianza, causando ciclos de retroalimentación negativa en la economía. Los impactos psicológicos pueden ser duraderos.
El seguimiento de contactos digitales podría desempeñar un papel fundamental para evitar o dejar el bloqueo. Hemos cuantificado el éxito esperado y hemos establecido una serie de requisitos para su implementación ética.
La aplicación que proponemos ofrece beneficios tanto para la sociedad como para las personas, reduciendo el número de casos y también permitiendo que las personas continúen sus vidas de una manera informada, segura y socialmente responsable. Ofrece el potencial para lograr importantes beneficios públicos al tiempo que maximiza la autonomía.
Existen problemas específicos para grupos dentro de la población que pueden no ser susceptibles a tal enfoque, y estos podrían ser rápidamente refinados en la política. Los trabajadores esenciales, como los trabajadores de la salud, pueden necesitar arreglos separados.
Se necesitan más modelos para comparar el número de personas interrumpidas en diferentes escenarios consistentes con la supresión de epidemia sostenida. Pero una pandemia sostenida no es inevitable, ni es un bloqueo nacional sostenido. Recomendamos la exploración urgente de medios para el distanciamiento físico inteligente a través del rastreo de contactos digitales.
Este es un artículo de acceso abierto distribuido bajo los términos de la licencia Creative Commons Attribution , que permite el uso, la distribución y la reproducción sin restricciones en cualquier medio, siempre que el trabajo original se cite correctamente.
Material suplementario.
Referencias y notas.
- y mate↵Organización Mundial de la Salud, Enfermedad por Coronavirus 2019 (COVID-19): Informe de situación – 36 (25 de febrero de 2020); www.who.int/docs/default-source/coronaviruse/situation-reports/20200225-sitrep-36-covid-19.pdf .Google Académico
- ↵ W.-J. Guan , Z.-Y. Ni , Y. Hu , W.-H. Liang , C.-Q. ou , J.-X. él , L. Liu , H. Shan , C.-L. Lei , DSC Hui , B. Du , L.-J. Li , G. Zeng , KENTUCKY. Yuen , R.-C. Chen , C.-L. Tang , T. Wang , P.-Y. Chen , J. Xiang , S.-Y. Li , J.-L. Wang, Z.-J. Liang , Y.-X. Peng , L. Wei , Y. Liu , Y.-H. Hu , P. Peng , J.-M. Wang , J.-Y. Liu , Z. Chen , G. Li , Z.-J. Zheng, S.-Q. Qiu , J. Luo , C.-J. ye , S.-Y. Zhu , N.-S. Zhong , Grupo de expertos en tratamiento médico de China para Covid-19, Características clínicas de la enfermedad por coronavirus 2019 en China . N. Engl. J. Med.10.1056 / NEJMoa2002032 ( 2020 ). doi: 10.1056 / NEJMoa2002032 pmid: 32109013 Cross Ref Pub Med Google Académico
- ↵H. Li, S. Wang, F. Zhong, W. Bao, Y. Li, L. Liu, H. Wang, Y. Él, riesgos de incidencia y mortalidad dependientes de la edad de COVID-19 en la provincia de Hubei y otras partes de China. medRxiv 2020.02.25.20027672 [preprint]. 6 de marzo de 2020.Google Académico
- ↵N. Ferguson, D. Laydon, G. Nedjati-Gilani, N. Imai, K. Ainslie, M. Baguelin, S. Bhatia, A. Boonyasiri, Z. Cucunubá, G. Cuomo-Dannenburg, A. Dighe, I. Dorigatti, H. Fu, K. Gaythorpe, W. Green, A. Hamlet, W. Hinsley, L. Okell, S. van Elsland, H. Thompson, R. Verity, E. Volz, H. Wang, Y. Wang , P. Walker, C. Walters, P. Winskill, C. Whittaker, C. Donnelly, S. Riley, A. Ghani, Impacto de las intervenciones no farmacéuticas (NPI) para reducir la mortalidad de COVID-19 y la demanda de asistencia sanitaria (16 de marzo 2020);www.imperial.ac.uk/media/imperial-college/medicine/sph/ide/gida-fellowships/Imperial-College-COVID19-NPI-modelling-16-03-2020.pdf .Google Académico
- ↵ SU Yu , JJY Sung, La epidemiología del brote del síndrome respiratorio agudo severo (SRAS) en Hong Kong: lo que sabemos y lo que no. Epidemiol Infectar. 132 , 781 – 786 ( 2004 ). doi: 10.1017 / S0950268804002614 pmid: 15473139 CrossRefPubMedGoogle Académico
- ↵Y. Li , X. Huang , SU Yu , TW Wong , H. Qian, Papel de la distribución del aire en la transmisión del SARS durante el mayor brote nosocomial en Hong Kong . Aire en espacios cerrados 15 , 83 – 95 ( 2005 ). doi:10.1111 / j.1600-0668.2004.00317.x pmid: 15737151 CrossRefPubMedWeb of ScienceGoogle Scholar
- ↵JA Otter , C. Donskey , S. Yezli , S. Douthwaite , SD Goldenberg , DJ Weber, Transmisión de coronavirus SARS y MERS y virus de la influenza en entornos sanitarios: el posible papel de la contaminación de la superficie seca . J. Hosp. Infectar. 92 , 235 – 250 ( 2016 ). doi: 10.1016 / j.jhin.2015.08.027 pmid: 26597631Cross Ref Pub Med Google Académico
- ↵SWX Ong , YK Tan , PY Chia , TH Lee , OT Ng , MSY Wong , K. Marimuthu, Aire, superficie ambiental y equipo de protección personal Contaminación por coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) de un paciente sintomático . JAMA 10.1001 / jama.2020.3227 ( 2020 ). doi: 10.1001 / jama.2020.3227 pmid: 32129805 Cross Ref Pub Med Google Académico
- ↵C. Fraser , S. Riley , RM Anderson , NM Ferguson, Factores que hacen que un brote de una enfermedad infecciosa controlable . Proc. Natl. Acad. Sci. Estados Unidos 101 , 6146 – 6151 ( 2004 ). doi: 10.1073 / pnas.0307506101 pmid: 15071187 Resumen / Texto completo GRATISGoogle Académico
- ↵CM Peak , LM Childs , YH Grad , CO Buckee, Comparación de intervenciones no farmacéuticas para contener epidemias emergentes . Proc. Natl. Acad. Sci. Estados Unidos 114 , 4023 – 4028 ( 2017 ). doi:10.1073 / pnas.1616438114 pmid: 28351976 Resumen / Texto completo GRATISGoogle Académico
- ↵J. Hellewell , S. Abbott , A. Gimma , NI Bosse , CI Jarvis , TW Russell , JD Munday , AJ Kucharski , WJEdmunds , S. Funk , RM Eggo , F. sol , S. Flasche , BJ Quilty , N. Davies , Y. Liu , S. Clifford , P. Klepac , M. Jit ,C. diamante , H. Gibbs , K. van Zandvoort , Centro de Modelado Matemático de Enfermedades Infecciosas Grupo de trabajo COVID-19, Viabilidad de controlar los brotes de COVID-19 mediante el aislamiento de casos y contactos . Lancet Glob. Salud 8 , e488 – e496 ( 2020 ). doi: 10.1016 / S2214-109X (20) 30074-7pmid: 32119825 Cross Ref Pub Med Google Académico
- ↵Q. Li , X. Guan , P. Wu , X. Wang , L. Zhou , Y. Tong , R. Ren , KSM Leung , EHY Lau ,JY Wong , X. Xing , N.Xiang , Y. Wu , C. Li , Q. Chen , D. Li , T. Liu , J. Zhao , M. Liu , W. Tu , C. Chen , L. Jin , R. Yang , Q. Wang , S.Zhou , R. Wang , H. Liu , Y. Luo , Y. Liu , G. Shao , H. Li , Z. Tao , Y. Yang , Z. Deng , B. Liu , Z. Ma , Y. Zhang , G.Shi , TTY Lam , JTK Wu , GF Gao , BJ Cowling , B. Yang , GM Leung , Z. Feng, Dinámica de transmisión temprana en Wuhan, China, de neumonía infectada por coronavirus novedoso . N. Engl. J. Med. 382 , 1199- 1207 ( 2020 ). doi: 10.1056 / NEJMoa2001316 pmid: 31995857 CrossRefPubMedGoogle Académico
- ↵Z.-D. Tong , A. Tang , K.-F. Li , P. Li , H.-L. Wang , J.-P. Yi , Y.-L. Zhang , J.-B. Yan, Transmisión presintomática potencial de SARS-CoV-2, provincia de Zhejiang, China, 2020 . Emerg. Infectar. Dis. 26 , (2020 ). doi: 10.3201 / eid2605.200198 pmid: 32091386 Cross Ref Pub Med Google Académico
- ↵Y. Bai , L. Yao , T. Wei , F. Tian , D.-Y. Jin , L. Chen , M. Wang, Presunta transmisión portadora asintomática de COVID-19 . JAMA 10.1001 / jama.2020.2565 ( 2020 ). doi: 10.1001 / jama.2020.2565 pmid: 32083643 Cross Ref Pub Med Google Académico
- ↵Channel News Asia; https://infographics.channelnewsasia.com/covid-19/coronavirus-singapore-clusters.html?cid=FBcna .Google Académico
- ↵Q. Bi, Y. Wu, S. Mei, C. Ye, X. Zou, Z. Zhang, X. Liu, L. Wei, SA Truelove, T. Zhang, W. Gao, C. Cheng, X. Tang , X. Wu, Y. Wu, B. Sun, S. Huang, Y. Sun, J. Zhang, T. Ma, J. Lessler, T. Feng, Epidemiología y transmisión de COVID-19 en Shenzhen, China: análisis de 391 casos y 1,286 de sus contactos cercanos.medRxiv 2020.03.03.20028423 [preimpresión]. 27 de marzo de 2020.Google Académico
- ↵K. Mizumoto , K. Kagaya , A. Zarebski , G. Chowell, Estimación de la proporción asintomática de casos de enfermedad por coronavirus 2019 (COVID-19) a bordo del crucero Diamond Princess, Yokohama, Japón, 2020 . Euro Surveill. 25 , ( 2020 ). doi: 10.2807 / 1560-7917.ES.2020.25.10.2000180 pmid:32183930 Cross Ref Pub Med Google Académico
- ↵R. Verity, LC Okell, I. Dorigatti, P. Winskill, C. Whittaker, N. Imai, G. Cuomo-Dannenburg, H. Thompson, P. Walker, H. Fu, A. Dighe, J. Griffin, A Cori, M. Baguelin, S. Bhatia, A. Boonyasiri, ZM Cucunuba, R. Fitzjohn, KAM Gaythorpe, W. Green, A. Hamlet, W. Hinsley, D. Laydon, G. Nedjati-Gilani, S. Riley. , S. van-Elsand, E. Volz, H. Wang, Y. Wang, X. Xi, C. Donnelly, A. Ghani, N. Ferguson, Estimaciones de la gravedad de la enfermedad COVID-19. medRxiv 2020.03.09.20033357 [preimpresión]. 13 de marzo de 2020.Google Académico
- ↵Y. Liu , L.-M. Yan , L. Wan , T.-X. Xiang , A. Le , J.-M. Liu , M. Peiris , LLM Poon , W. Zhang, Dinámica viral en casos leves y severos de COVID-19 . Lancet Infect. Dis. S1473-3099 (20) 30232-2 ( 2020 ). doi: 10.1016 / S1473-3099 (20) 30232-2 pmid: 32199493 CrossRefPubMedGoogle Académico
- ↵I. Dorigatti, L. Okell, A. Cori, N. Imai, M. Baguelin, S. Bhatia, A. Boonyasiri, Z. Cucunubá, G. Cuomo-Dannenburg, R. FitzJohn, H. Fu, K. Gaythorpe, A. Hamlet, W. Hinsley, N. Hong, M. Kwun, D. Laydon, G. Nedjati-Gilani, S. Riley, S. van Elsland, E. Volz, H. Wang, R. Wang, C. Walters , X. Xi, C. Donnelly, A. Ghani, N. Ferguson, Informe 4: Severidad del nuevo coronavirus 2019 (nCoV) (10 de febrero de 2020);www.imperial.ac.uk/media/imperial-college/medicine/sph/ide/gida-fellowships/Imperial-College-COVID19-severity-10-02-2020.pdf .Google Académico
- ↵SA Lauer, KH Grantz, Q. Bi, FK Jones, Q. Zheng, H. Meredith, AS Azman, NG Reich, J. Lessler, El período de incubación de 2019-nCoV a partir de casos confirmados informados públicamente: Estimación y aplicación. medRxiv 2020.02.02.20020016 [preprint]. 4 de febrero de 2020.Google Académico
- ↵H. Nishiura, NM Linton, AR Akhmetzhanov, Intervalo en serie de nuevas infecciones por coronavirus (2019-nCoV). medRxiv 2020.02.03.20019497 [preprint]. 17 de febrero de 2020. Google Académico
- ↵NC Grassly , C. Fraser, Modelos matemáticos de transmisión de enfermedades infecciosas . Nat. Rev. Microbiol. 6 , 477 – 487 ( 2008 ). doi: 10.1038 / nrmicro1845 pmid: 18533288 CrossRefPubMedWeb of ScienceGoogle Scholar
- ↵BDI Pathogen Dynamics Group, seguimiento de contactos digitales para SARS-COV-2 (2020);https://bdi-pathogens.shinyapps.io/covid-19-transmission-routes/ .Google Académico
- ↵P. Mozur, R. Zhong, A. Krolik, “En la lucha contra el coronavirus, China da a los ciudadanos un código de color, con banderas rojas”. New York Times (1 de marzo de 2020);www.nytimes.com/2020/03/01/business/china-coronavirus-surveillance.html .Google Académico
- ↵S. Chen , J. Yang , W. Yang , C. Wang , T. Bärnighausen, Control COVID-19 en China durante los movimientos masivos de población en Año Nuevo . Lancet 395 , 764 – 766 ( 2020 ). doi: 10.1016 / S0140-6736 (20) 30421-9 pmid: 32105609 CrossRefPubMedGoogle Académico
- ↵Consejo Nuffield de Bioética, Investigación en emergencias sanitarias mundiales: cuestiones éticas (28 de enero de 2020); www.nuffieldbioethics.org/publications /research-in-global-health-emergencies .Google Académico
- ↵S. Zhao , Q. Lin , J. Ran , SS Musa , G. Yang , W. Wang , Y. Lou , D. Gao , L. Yang , D. El , MH Wang,Estimación preliminar del número de reproducción básica del nuevo coronavirus (2019-nCoV) en China, de 2019 a 2020: un análisis basado en datos en la fase temprana del brote . En t. J. Infect. Dis. 92 , 214 – 217 (2020 ). doi: 10.1016 / j.ijid.2020.01.050 pmid: 32007643 Cross Ref Pub Med Google Académico
- ↵T. Zhou , Q. Liu , Z. Yang , J. Liao , K. Yang , W. Bai , X. Lu , W. Zhang, Predicción preliminar del número de reproducción básico del nuevo coronavirus de la novela de Wuhan 2019-nCoV . J. Evid. Med. Basada 13 , 3- 7 ( 2020 ). doi: 10.1111 / jebm.12376 pmid: 32048815 CrossRefPubMedGoogle Académico
- ↵T. Ganyani, C. Kremer, D. Chen, A. Torneri, C. Faes, J. Wallinga, N. Hens, Estimando el intervalo de generación para COVID-19 basado en datos de inicio de síntomas. medRxiv 2020.03.05.20031815[preprint]. 8 de marzo de 2020.Google Académico
- ↵X. Él, EHY Lau, P. Wu, X. Deng, J. Wang, X. Hao, YC Lau, JY Wong, Y. Guan, X. Tan, X. Mo, Y. Chen, B. Liao, W Chen, F. Hu, Q. Zhang, M. Zhong, Y. Wu, L. Zhao, F. Zhang, BJ Cowling, F. Li, GM Leung, Dinámica temporal en la eliminación viral y transmisibilidad de COVID-19. medRxiv 2020.03.15.20036707 [preprint].18 de marzo de 2020.Google Académico
- ↵D. Klinkenberg , C. Fraser , H. Heesterbeek, La efectividad del rastreo de contactos en epidemias emergentes . PLOS ONE 1 , e12 ( 2006 ). doi: 10.1371 / journal.pone.0000012 pmid: 17183638 CrossRefPubMedGoogle Académico
- ↵M. Salathé , M. Kazandjieva , JW Lee , P. Levis , MW Feldman , JH Jones, Una red de contacto humano de alta resolución para la transmisión de enfermedades infecciosas . Proc. Natl. Acad. Sci. Estados Unidos107 , 22020 – 22025 ( 2010 ). doi: 10.1073 / pnas.1009094108 pmid: 21149721 Resumen / Texto completo GRATIS Google Académico
- E. Yoneki , J. Crowcroft, EpiMap: hacia la cuantificación de redes de contacto para comprender la epidemiología en los países en desarrollo . Ad Hoc Netw. 13 , 83 – 93 ( 2014 ). doi: 10.1016 / j.adhoc.2012.06.003 CrossRefGoogle Scholar
- ↵KA Nguyen, Z. Luo, C. Watkins, en progreso en los servicios basados en la ubicación 2014 , G. Gartner, H. Huang, Eds. (Springer, 2015), págs. 63–78.Google Académico
- ↵GM Leung , P.-. Chung , T. Tsang , W. Lim , SKK Chan , P. Chau , CA Donnelly , AC Ghani , C. Fraser , S.Riley , NM Ferguson , RM Anderson , Y.-L. Ley , T. Mok , T. Ng , A. Fu , P.- Leung , JSM Peiris , T.-H. Lam , AJHedley, Prevalencia de anticuerpos contra el SARS-CoV en todos los contactos de pacientes de Hong Kong. Emerg. Infectar. Dis. 10 , 1653 – 1656 ( 2004 ) . doi: 10.3201 / eid1009.040155 pmid: 15498170 Cross Ref Pub Med Web of Science Google Scholar
- ↵K.-Q. Kam , CF Yung , L. Cui , R. Tzer Pin Lin , TM Mak , M. Maiwald , J. Li , CY Chong , K. Nadua , NWHTan , KC Thoon, Un bebé sano con enfermedad por coronavirus 2019 con alta carga viral . Clin. Infectar. Dis.ciaa201 ( 2020 ). doi: 10.1093 / cid / ciaa201 pmid: 32112082 Cross Ref Pub Med Google Académico
- ↵X. Lu , L. Zhang , H. Du , J. Zhang , YY Li , J. Qu , W. Zhang , Y. Wang , S. Bao , Y. Li , . Wu , H. Liu , D. Liu ,J. Shao , X. Peng , Y. Yang , Z. Liu , Y. Xiang , F. Zhang , RM Silva , KE Pinkerton , K. Shen , H. Xiao , S. Xu , GWK Wong, Infección por SARS-CoV-2 en niños . N. Engl. J. Med. NEJMc2005073 ( 2020 ). doi: 10.1056 / NEJMc2005073 pmid: 32187458 Cross Ref Pub Med Google Académico
- G. Kampf , D. Todt , S. Pfaender , E. Steinmann, Persistencia de coronavirus en superficies inanimadas y su inactivación con agentes biocidas . J. Hosp. Infectar. 104 , 246 – 251 ( 2020 ). doi: 10.1016 / j.jhin.2020.01.022 pmid: 32035997 Cross Ref Pub Med Google Académico
- ↵El código utilizado para nuestros análisis está disponible en https://doi.org/10.5281/zenodo.3727255. Google Académico
- ↵L. Ferretti, C. Wymant, M. Kendall, L. Zhao, A. Nurtay, DG Bonsall, C. Fraser, La cuantificación de la dinámica de la transmisión del SARS-CoV-2 sugiere que el control y la evitación de epidemias es factible a través del rastreo instantáneo de contactos digitales. medRxiv 2020.03.08.20032946 [preimpresión]. 12 de marzo de 2020.Google Académico
- Centro de China para el Control de Enfermedades, Distribución de Neumonía por Nuevo Coronavirus;http://2019ncov.chinacdc.cn/2019-nCoV/ .Google Académico
- LT Phan , TV Nguyen , QC Luong , TV Nguyen , HT Nguyen , HQ Le , TT Nguyen , TM Cao , QD Pham,Importación y transmisión de humano a humano de un nuevo coronavirus en Vietnam . N. Engl. J. Med.382 , 872 – 874 ( 2020 ). doi: 10.1056 / NEJMc2001272 pmid: 31991079 Cross Ref Pub Med Google Académico
- M. Ki , Fuerza de Tarea para 2019-nCoV, Características epidemiológicas de los primeros casos con la enfermedad del nuevo coronavirus 2019 (2019-nCoV) en la República de Corea . Epidemiol Salud 42 ,e2020007 ( 2020 ). doi: 10.4178 / epih.e2020007 CrossRefGoogle Scholar
- ↵C. Rothe , M. Schunk , P. Sothmann , G. Bretzel , G. Froeschl , C. Wallrauch , T. Zimmer , V. Thiel , C. Janke, W. Guggemos , M. Seilmaier , C. Drosten , P. Vollmar , K. Zwirglmaier , S. Zange , R. Wölfel , M. Hoelscher,Transmisión de la infección 2019-nCoV desde un contacto asintomático en Alemania . N. Engl. J. Med. 382, 970 – 971 ( 2020 ). doi: 10.1056 / NEJMc2001468 pmid: 32003551 Cross Ref Pub Med Google Académico
Agradecimientos: Agradecemos a Will Probert, Andrei Akhmetzhanov, Alice Ledda, Ben Cowling, Gabriel Leung y Yuan Yang por sus útiles comentarios. Financiación: Este trabajo fue financiado por la Fundación Li Ka Shing. AN está financiado por Artic Network (Premio Wellcome Trust Collaborators 206298 / Z / 17 / Z). Los financiadores no jugaron ningún papel en la concepción o ejecución del estudio. Contribuciones de los autores: Conceptualización: CF, DB. Conservación de datos: LF, CW, AN, LZ. Adquisición de fondos: CF, MP. Investigación: LF, CW, MK, CF. Metodología: LF, CW. Visualización: LF, CW, MK, DB. Administración del proyecto: LA. Software: MK. Análisis ético: MP, CF, DB. Redacción, borrador original: LF, CW, MP, DB, CF. Redacción, revisión y edición: todos los autores. Conflicto de intereses: ninguno declarado.Disponibilidad de datos y materiales:Todos los datos están disponibles en el manuscrito o en el material complementario. El código utilizado para nuestros análisis está disponible públicamente en ( 40 ). Este trabajo está licenciado bajo una licencia Creative Commons Attribution 4.0 International (CC BY 4.0), que permite el uso, la distribución y la reproducción sin restricciones en cualquier medio, siempre que el trabajo original se cite correctamente. Para ver una copia de esta licencia, visite https://creativecommons.org/licenses/by/4.0/ . Esta licencia no se aplica a figuras / fotos / obras de arte u otro contenido incluido en el artículo que se acredite a un tercero; obtener autorización del titular de los derechos antes de usar dicho material.










Deja un comentario