El 12 de marzo de 2026 se conmemora el Día del Riñón, una fecha dedicada a crear conciencia sobre la salud renal y la prevención de factores de riesgo como la diabetes y la hipertensión. Desde Bayer, a través de la campaña RenalMente Importante, resaltamos la carga que enfrentan pacientes y cuidadores, incorporando también mi experiencia personal acompañando a una paciente en terapia de reemplazo renal
Según la Cuenta de Alto Costo (CAC) 2024, en Colombia se registraron 1.251.930 casos prevalentes de enfermedad renal crónica (ERC), un incremento del 26,3% frente a 2023, y 281.715 casos incidentes, que representan un aumento del 40,7%[1]. La CAC destaca que las mujeres son proporcionalmente más afectadas, lo que obliga a analizar los factores de riesgo específicos en ellas, especialmente durante marzo, mes en el que se conmemora la histórica lucha por sus derechos y equidad[2]. De acuerdo con el Global Burden of Disease 2023, la prevalencia de ERC en mujeres es 1,2 a 1,4 veces mayor que en los hombres[3], debido a determinantes biológicos, hormonales y psicosociales. La pérdida estrogénica posmenopáusica[4],[5], enfermedades metabólicas como diabetes e hipertensión[6],[7], y condiciones autoinmunes como lupus o inmunes contribuyen a un mayor riesgo de progresión renal[8]. Asimismo, factores reproductivos como la preeclampsia pueden triplicar el riesgo de desarrollar ERC[9]. Reconocer estas diferencias es esencial para mejorar la prevención, el diagnóstico temprano y el abordaje integral de la ERC en Colombia.
La ERC representa una de las cargas globales de enfermedad más altas, expresada en años saludables perdidos por muerte prematura y discapacidad (DALYs, por sus siglas en inglés), y su impacto varía significativamente según la causa subyacente y aumenta de manera exponencial conforme avanza el estadio renal, siendo el estadio 4 y, especialmente, el estadio 517,26. La diabetes mellitus, actualmente la principal etiología de ERC a nivel mundial concentra más del 40% de los DALYs atribuidos a ERC debido a su progresión más rápida, alta mortalidad cardiovascular asociada y elevada discapacidad funcional, generando tasas de DALYs entre 1.5 y 2 veces mayores que las de ERC secundaria a hipertensión u otras causas específicas12,14,[10]. En contraste, la ERC de causa no conocida —que puede representar entre el 15 y 25% de los casos en cohortes globales— se asocia con una carga de enfermedad igualmente elevada debido a progresión silenciosa, menor adherencia terapéutica dirigida y mayor incertidumbre clínica[1],[2]
Ranking de la carga de la enfermedad de la ERC por diferentes causas en términos de DALYs por 100.000 para ambos géneros y todas las edades en 2023 a nivel mundial.
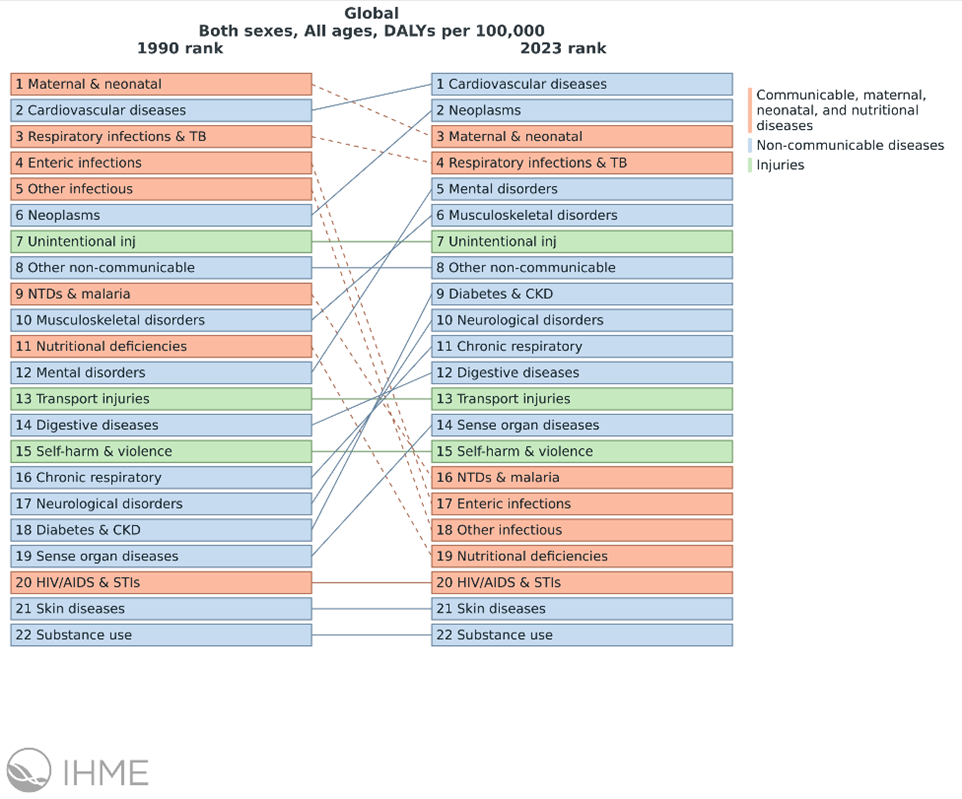
Fuente: Institute for Health Metrics and Evaluation (IHME). GBD 2023 Results. Seattle, WA: IHME, University of Washington; 2023. Disponible en: https://vizhub.healthdata.org/gbd-results
Centrándonos sólo en las personas fallecidas con diagnóstico asociado (causa directa de ERD), utilizando Estadísticas Vitales de DANE con un enfoque diferente al de la Cuenta de Alto Costo en Colombia, se determinó que, del total de fallecimientos por muerte natural en el año 2022 (236 mil personas en total) el 0.45% (1,145 personas) tuvieron como causa directa ERD, lo cual desde el 2021 se observa una pendiente creciente.
Proporción de Fallecidos ERD respecto a Muertes Naturales
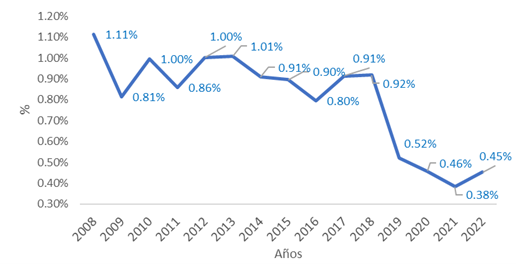
Fuente: Cálculos realizados con microdatos de Estadísticas Vitales DANE. 2008-2022[1]
Desde una perspectiva de causalidad, la Cuenta de Alto Costo (CAC) reporta que en Colombia solo el 35,45% de los casos de ERC tienen una etiología definida: 16,99% corresponden a enfermedad vascular renal y 10,11% a diabetes mellitus, mientras que el 45,56% carece de diagnóstico etiológico y el 18,99% no cuenta con causa especificada. Esta ausencia de etiología clara es clínicamente relevante, pues los pacientes con ERC de causa desconocida presentan mayor riesgo de progresión, menor uso de terapias renoprotectoras y mayor mortalidad comparados con quienes tienen un diagnóstico definido[1],[2]. En contraste, cuando la ERC se atribuye a hipertensión o diabetes —responsables del 75–80% de los casos globales según GBD 2023— es posible instaurar intervenciones de alto impacto, como control intensivo de la presión arterial, manejo glucémico, iSGLT2, ARM finerenona y bloqueo del SRAA, logrando reducciones del 30–40% en la progresión a enfermedad renal terminal[3],[4],[5],[6].
La ausencia de un diagnóstico etiológico en la enfermedad renal crónica no solo retrasa la referencia a nefrología y reduce el tamizaje de complicaciones, sino que también favorece el subtratamiento en atención primaria[7]. A nivel poblacional, esta falta de claridad limita la vigilancia epidemiológica, afecta la planeación sanitaria y subestima la carga prevenible atribuible a hipertensión y diabetes, un reto especialmente relevante para países como Colombia[8],[9]. En el ámbito familiar, no conocer la causa del deterioro renal incrementa la incertidumbre y la carga emocional del cuidador, reflejada en aumentos de 8–12 puntos en el Zarit Burden Interview (ZBI) [10],[11] y 20–30% en el Caregiver Strain Index (CSI), además de mayor frecuencia de síntomas ansioso‑depresivos medidos por la Escala de Ansiedad y Depresión Hospitalaria (HADS) [12],[13],[14]. En contraste, los cuidadores de pacientes con ERC atribuida a diabetes o hipertensión presentan menor carga percibida gracias a planes terapéuticos más claros, mientras que aquellos que acompañan a personas con etiologías desconocidas reportan incrementos del 20–35% en carga total y mayor incertidumbre clínica, evidenciada también en diferencias significativas en ZBI y CSI19,20,[15].
La importancia de analizar la ERC desde su carga clínica y económica se evidencia en el marcado aumento de casos por estadio entre 2022 y 2024: los estadios 1 y 2 crecieron 36,7% y 37,6%, mientras que los estadios 3 y 4 aumentaron más del 24%1. De forma particularmente preocupante, los casos nuevos en estadio 5 se incrementaron 177%, y su prevalencia aumentó 8,65%, con un 41% atribuible a diabetes sola o combinada con hipertensión1. Este estadio, la fase más avanzada de la enfermedad, concentra una de las cargas más altas entre las patologías crónicas, con deterioro funcional severo, alta multimorbilidad y pérdidas del 50–60% en calidad
de vida medida por EQ‑5D, además de mayor frecuencia de hospitalizaciones y mortalidad[1],[2]. Para los cuidadores, el estadio 5 implica una carga sustancial: incrementos de 15–20 puntos en ZBI, 30–40% en CSI19,[3],[4] y mayores niveles de ansiedad, depresión y agotamiento medidos por HADS, especialmente en contextos de diálisis frecuente y alta dependencia23,[5]. En Colombia, la CAC confirma que el estadio 5 concentra más del 65% de los costos directos del manejo renal, en paralelo con el crecimiento sostenido de la población en diálisis y la creciente demanda emocional, logística y económica sobre pacientes y cuidadores1. Esta realidad también se refleja en mi experiencia personal como cuidadora, enfrentando no solo el impacto clínico, sino también la carga emocional, las exigencias logísticas y las afectaciones laborales y económicas asociadas al acompañamiento cotidiano.
Además, del estadio determinado por la tasa de filtración glomerular, la medición de albuminuria y de la relación albúmina‑creatinina (RAC) es clave para estratificar el riesgo renal y cardiovascular, especialmente en la enfermedad renal diabética, donde una RAC elevada puede duplicar el riesgo de progresión y triplicar la probabilidad de requerir diálisis17,[6]. La albuminuria anticipa pérdida acelerada del filtrado glomerular y una trayectoria clínica que favorece hospitalizaciones y transición temprana a estadios 4–5[7]. Para el paciente y su familia, un resultado elevado genera mayor ansiedad y ajustes estrictos en el cuidado ante la posibilidad de diálisis29. Para el cuidador, una RAC aumentada se asocia con mayor carga emocional y logística, reflejada en incrementos 8–12 puntos en la escala ZBI, 20–30% en la escala CSI y síntomas ansiosos‑depresivos evaluados con HADS26,29,30. Por ello, medir albuminuria y RAC no es únicamente una recomendación clínica: es una intervención costo‑efectiva que permite anticipar complicaciones, reducir la progresión hacia diálisis y mitigar la carga física, emocional y económica que recae simultáneamente sobre el paciente y su cuidador.
Frente a este panorama, la enfermedad renal crónica no solo representa un reto clínico y epidemiológico, sino también un recordatorio del peso silencioso que soportan miles de familias y cuidadores en Colombia. Detrás de cada cifra hay una historia: un paciente que enfrenta determinantes biológicos y sociales que amplifican su vulnerabilidad, un cuidador que ajusta su vida para sostener la esperanza, y un hogar que reorganiza rutinas, finanzas y emociones frente a un tratamiento que exige presencia constante. La carga de enfermedad trasciende DALYs y prevalencias: cada avance de estadio transforma vidas y desgasta a quienes acompañan el proceso. La evidencia es clara: identificar la etiología, intervenir temprano en diagnóstico, promover tratamientos integrales y fortalecer los sistemas de cuidado, modifica la trayectoria clínica y reduce el sufrimiento evitable del paciente y su entorno.
[1] Cuenta de Alto Costo (CAC). Fondo Colombiano de Enfermedad de Alto Costo. Situación de la Enfermedad Renal Crónica, hipertensión arterial y la diabetes mellitus en Colombia. 2024; Bogotá, D.C. 2025
[2] Naciones Unidas. Día Internacional de la Mujer, 8 de marzo. Antecedentes. Historia del Día de la Mujer. URL: https://www.un.org/es/observances/womens-day/background
[3] Institute for Health Metrics and Evaluation (IHME). GBD 2023 Results. Seattle, WA: IHME, University of Washington; 2023. Disponible en: https://vizhub.healthdata.org/gbd-results.
[4] Neugarten J, Golestaneh L. Sex differences in renal disease: the role of estrogens. J Am Soc Nephrol. 2018;29(10):2547–2556.
[5] Carrero JJ, Hecking M, Chesnaye NC, Jager KJ. Sex and gender disparities in chronic kidney disease: progression to end-stage renal disease and dialysis initiation. Kidney Int. 2018;94(2):260–264.
[6] Peters SAE, Woodward M. Sex differences in the burden and complications of diabetes. Lancet Diabetes Endocrinol. 2014;2(6):498–506.
[7] Whelton PK, Carey RM, Aronow WS, et al. Hypertension and risk of renal outcomes: clinical practice implications. Hypertension. 2022;79(5):e21–e27.
[8] Almaani S, Meara A, Rovin BH. Update on lupus nephritis. Lancet. 2023;402(10388):123–139.
[9] McDonald SD, Malinowski A, Zhou Q, Yusuf S, Devereaux PJ. Kidney disease after preeclampsia: a systematic review and meta-analysis. BMJ. 2022;365:l1516.
[10] Jha V, Garcia-Garcia G, Iseki K, et al. Chronic kidney disease: updated global patterns and risks. Lancet. 2023;402(10414):1781–1796.
[11] Eneanya ND, Mariani LH, Bomback AS. Diagnostic uncertainty in CKD and implications for disease burden. Nat Rev Nephrol. 2022;18(9):559–572.
[12] Stanifer JW, Luyckx VA, Al-Aly Z. CKD in low- and middle-income countries: shifting patterns. Kidney Int. 2023;103(6):1230–1242.
[13] Departamento Administrativo Nacional de Estadística (DANE). Estadísticas Vitales: Defunciones no fetales, Colombia 2022. Bogotá: DANE; 2023. Disponible en: https://www.dane.gov.co/index.php/estadisticas-por-tema/salud/estadisticas-vitales
[14] Levin A, Tonelli M,Bonventre J, et al. Global kidney health 2023: progress and gaps in CKD diagnosis. Kidney Int. 2023;104(1):3–15.
[15] Eneanya ND, Mariani LH, Bomback AS. Diagnostic uncertainty in CKD: consequences for management and outcomes. Nat Rev Nephrol. 2022;18(9):559–572.
[16] Institute for Health Metrics and Evaluation (IHME). GBD 2023 Results. Seattle, WA: IHME, University of Washington; 2023. Disponible en: https://vizhub.healthdata.org/gbd-results
[17] Cockwell P, Luyckx VA. The growing global burden of CKD: updated epidemiology 2023. Lancet. 2023;402(10414):1781–1796.
[18] Kidney Disease: Improving Global Outcomes (KDIGO). KDIGO 2022 Clinical Practice Guideline for Diabetes in CKD. Kidney Int Suppl. 2022;12(1):1–115.
[19] Agarwal R, Anker SD, Filippatos G, Pitt B, et al. Kidney outcomes with finerenone and SGLT2 inhibitors in CKD: updated pooled analyses. N Engl J Med. 2023;388(19):2155–2167.
[20] Bello AK, Johnson DW, Feehally J. Delayed nephrology referral and suboptimal CKD management: updated global evidence 2021–2024. Clin Kidney J. 2024;17(2):285–296.
[21] GBD Chronic Kidney Disease Collaboration. Global, regional, and national burden of CKD, 1990 2023: systematic analysis. Lancet. 2024;403(10512):1125–1144.
[22] Stanifer JW, Luyckx VA, Al-Aly Z. CKD in low- and middle-income countries: shifting patterns and health system implications. Kidney Int. 2023;103(6):1230–1242.
[23] Tsai YC, Hung CC, Hwang SJ, et al. Caregiver burden in CKD: differences by disease certainty and treatment trajectory. Nephrology (Carlton). 2022;27(3):215–224.
[24] Al-Rawashdeh SY, Lennie TA, Chung ML. The association of uncertainty with burden in caregivers of patients with chronic illnesses: updated evidence for nephrology. J Clin Nurs. 2023;32(7–8):1985–1994.
[25] Khalil AA, Abed MA, Jarrah S. Psychological distress and caregiver strain among caregivers of CKD patients: a cross-sectional analysis. BMC Nephrol. 2021;22(1):447.
[26] Kang AW, Kim H, Choi KH. Impact of unclear etiology of CKD on caregiver strain and mental health outcomes. Clin Kidney J. 2024;17(1):112–120.
[27] Torrisi L., et al. Patient and caregiver perspectives on mental health in children and adolescents with chronic kidney disease. Patient and caregiver perspectives on mental health in children and adolescents with chronic kidney disease. Clin Kidney J. 2025 Mar 8;18(4):sfaf067.
[28] Martínez‑Fernández B, López‑Revuelta K, Pérez‑Gómez MV. Caregiver experience in CKD due to hypertension and diabetes: psychological and functional differences. J Ren Care. 2023;49(4):266–275.
[29] GBD Chronic Kidney Disease Collaboration. Global, regional, and national burden of CKD, 1990–2023: systematic analysis. Lancet. 2024;403(10512):1125–1144.
[30] Purnell TS, Auguste P, Crews DC, et al. Patient-reported outcomes across CKD stages: updated meta-analysis 2023. Kidney Int. 2023;104(5):901–913.
[31] Kang AW, Kim H, Choi KH. Impact of CKD stage 5 on caregiver strain: cross-sectional comparison using ZBI and CSI. Clin Kidney J. 2024;17(1):112–120.
[32] López‑Revuelta K, Martínez‑Fernández B, Pérez‑Gómez MV. Caregiver burden and dependency in advanced CKD: findings from contemporary nephrology practice. J Ren Care. 2023;49(4):266–275.
[33] Bello AK, Johnson DW, Feehally J. Global caregiving challenges in advanced CKD: socioeconomic and health system impacts. Clin Kidney J. 2024;17(2):285–296.
[34] Perkovic V, Jardine MJ, Neal B, et al. Canagliflozin and renal outcomes in type 2 diabetes (CREDENCE). N Engl J Med. 2019;380:2295–306.
[35] Herrington WG, Staplin N, Wanner C, et al. Empagliflozin in patients with chronic kidney disease (EMPA‑KIDNEY). Lancet. 2023;401:213–25.







Deja un comentario